|
|
Los electrones se encuentran en la periferia del átomo. Tienen una masa y un tamaño mucho menor que el de los nucleones.  Pero, ¿por qué
los electrones no son atraídos por el núcleo y colapsan en
él?.
|
|
| Porque los electrones, colocados
en la periferia del átomo, tienen zonas restrigidas de movimiento,
denominadas orbitales atómicos. |
||
|
Los orbitales atómicos se distribuyen en capas alrededor del núcleo y tienen formas diferentes. Los orbitales s son esféricos. En la capa 1 sólo hay orbitales s. En la capa 2 hay orbitales s y p. Estos últimos tienen una forma parecida al contorno de dos globos unidos por la boca de llenado. En las siguientes capas el tipo de orbitales y su forma se complica aun más. |
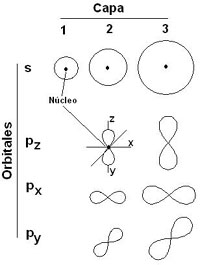
Los orbitales aquí representados se encuentran superpuestos alrededor del núcleo. Se muestran separadamente para aumentar la claridad del dibujo. |
Los orbitales atómicos son como las
rutas aéreas de los aviones que, aunque invisibles, están fijadas para evitar colisiones. Cuanto más alejados del núcleo, los orbitales ocupan más espacio. |