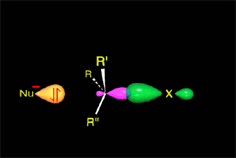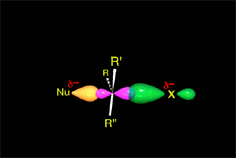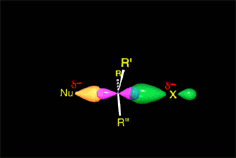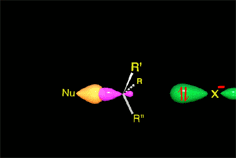Se pueden entender las reacciones entre las moléculas en función de la densidad electrónica que poseen. La densidad electrónica, al igual que la presión en la atmósfera (borrascas -baja presión- y anticiclones -alta presión-), no se reparte por igual en las moléculas. Los átomos electronegativos "concentran" densidad electrónica a su alrededor y "desnudan" de densidad electrónica a los átomos próximos.
El anión hidróxido (HO-) proviene del agua por pérdida de un protón. Tiene una gran densidad electrónica. Es el nucleófilo (rojo). Reacciona con el cloruro de metilo atacando la molécula por el lado del metilo que, por culpa del cloro, tiene un defecto de densidad electrónica. Es el electrófilo (azul). Se rompe el enlace C-Cl y se forma el enlace C-O. El enlace C-O es más fuerte que el C-Cl y la reacción es energéticamente favorable.
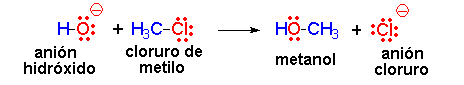
 Distribución electrónica en el cloruro de metilo (roja = alta; azul = baja)
Distribución electrónica en el cloruro de metilo (roja = alta; azul = baja)