A) ciclopropano < ciclobutano < ciclohexano < ciclopentano
B) ciclohexano < ciclopentano < ciclobutano < ciclopropano
C) ciclohexano < ciclobutano < ciclopentano < ciclopropano
D) ciclopentano < ciclopropano < ciclobutano < ciclohexano
E) ciclopropano < ciclopentano < ciclobutano < ciclohexano
B) ciclohexano < ciclopentano < ciclobutano < ciclopropano
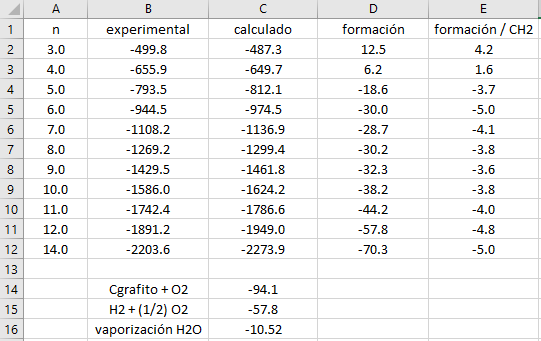
Calcula los calores de combustión de los cicloalcanos hasta 14 miembros y, a partir de los calores experimentales de la tabla, calcula los calores de formación correspondientes. Da una breve explicación a los valores obtenidos.
El ciclopropano y el ciclobutano son estructuras menos estables que sus átomos de partida porque sus calores de formación son positivos.
Estos cicloalcanos, sobre todo el ciclopropano, tienen tensión de enlace porque sus ángulos internos (60º y 90º) son mucho más pequeños que los "naturales" del tetrahedro (109,5º) que forma un carbono en hibridación sp3.
Estos cicloalcanos, sobre todo el ciclopropano, tienen tensión de eclipsamiento entre los hidrógenos de grupos CH2 contiguos.
El ciclohexano es el cicloalcano más pequeño donde el calor de formación por grupo CH2 es
más pequeño y, por tanto, es el más estable.
El ciclohexano en su conformación silla tiene ángulos de enlace C-C-C (aprox. 108º) muy parecidos al tetraédrico "natural" y todos los grupos CH2 están perfectamente alternados.
El ángulo interno de un ciclopentano es casi como el tetraédrico pero, a diferencia del ciclohexano, NO puede adoptar una forma "silla" y las tensiones de eclipsamiento se mantienen.
El anillo tiene que ser tan grande como de 14 carbonos para que se consiga una situación de estabilidad como la del ciclohexano. Los cicloalcanos entre éste y el ciclotetradecano siempre tienen algo de tensión de eclipsamiento que hace que los calores de formación por grupo CH2 no sean tan negativos.