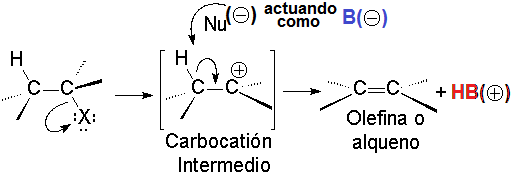
ELIMINACIÓN UNIMOLECULAR (E1)
El carbocatión producido por la salida del halógeno o en general, del grupo saliente, puede tener una evolución alternativa a la reacción SN1: la eliminación de un protón en posición contigua
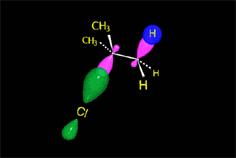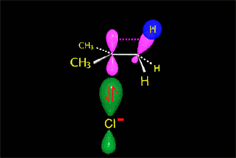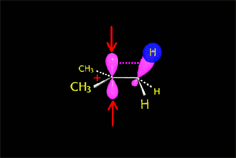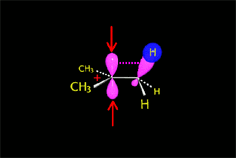 Carbocatión (SN1)
Carbocatión (SN1)
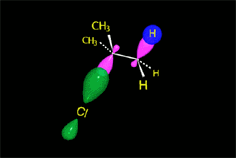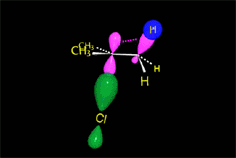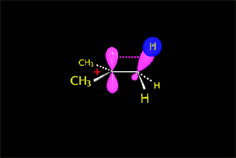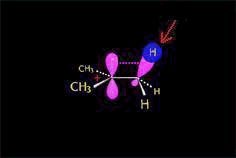 Carbocatión (E1)
Carbocatión (E1)
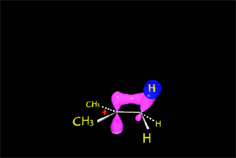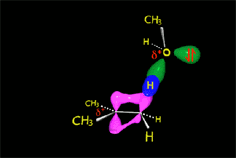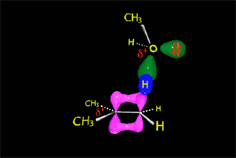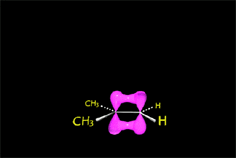
El nucleófilo, actuando como base, puede extraer un protón del carbono adyacente al carbocatión, dando lugar a una olefina.
En el caso de la metanolisis del cloruro de terc-butilo es el metanol el que actúa como base, se lleva el protón y da lugar a isobutileno.
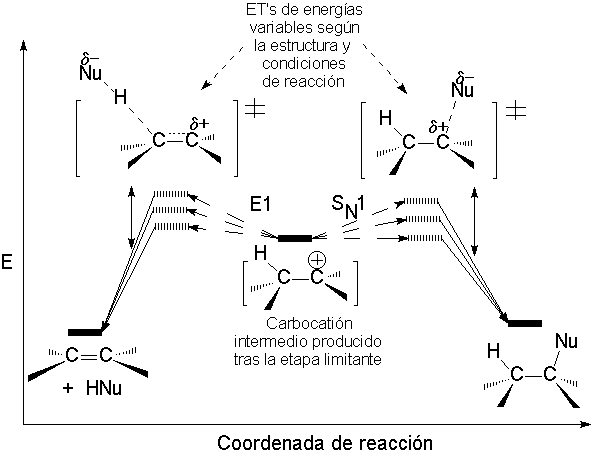
Por tanto, una vez producido el carbocatión, éste puede evolucionar de dos maneras. El diagrama cualitativo de energía es el siguiente:
La proporción entre sustitución y eliminación no depende del grupo saliente porque el carbocatión formado es el mismo, pero sí de la relación basicidad-nucleofilia de la base-nucleófilo atacante.
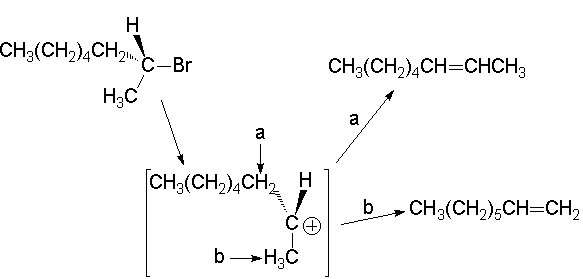
Cualquier hidrógeno contiguo al carbono que soporta el grupo saliente puede participar en la reacción E1. Por tanto, en el carbocatión generado a partir del 2-bromooctano se pueden obtener dos olefinas, el 1- y el 2-octeno:
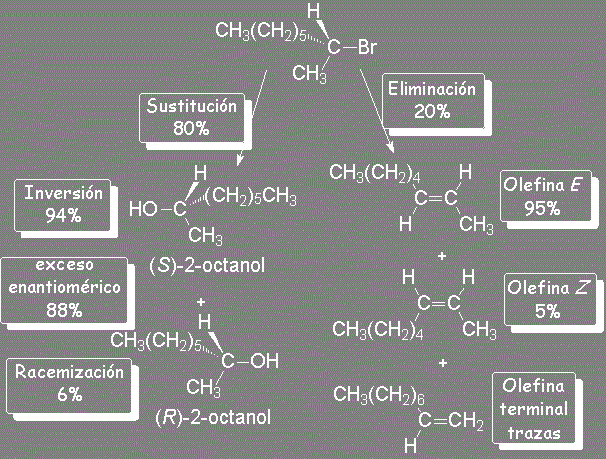
Con lo que hemos explicado por qué se obtienen las olefinas de nuestro experimento.
Queda por saber por qué el 1-octeno se obtiene en mucha menor proporción y por qué el 2-octeno se obtiene en configuración E (trans) mayoritariamente. Tendremos que esperar al capítulo de alquenos para comprenderlo.
 Carbocatión (SN1)
Carbocatión (SN1)
 Carbocatión (E1)
Carbocatión (E1)