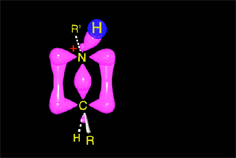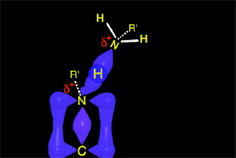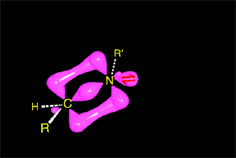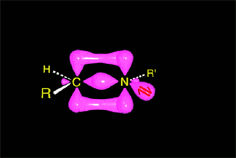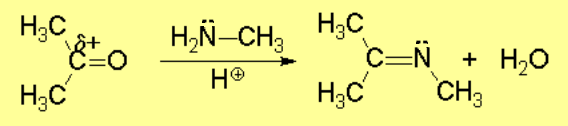
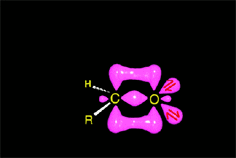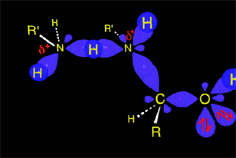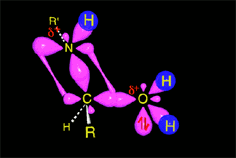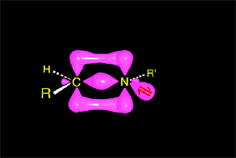
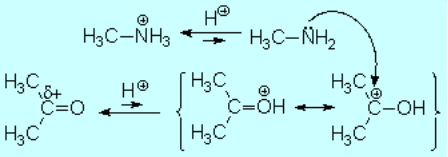
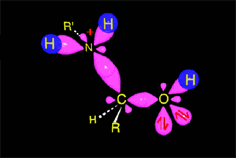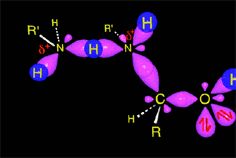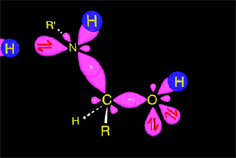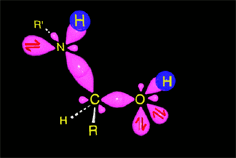
 La catálisis ácida produce la protonación de algunas moléculas de cetona, aumentando la electrofilia del carbono carbonílico. Se produce entonces la adición nucleófila del nitrógeno amínico sobre el carbono carbonílico, que cambia de hibridación sp2 a sp3.
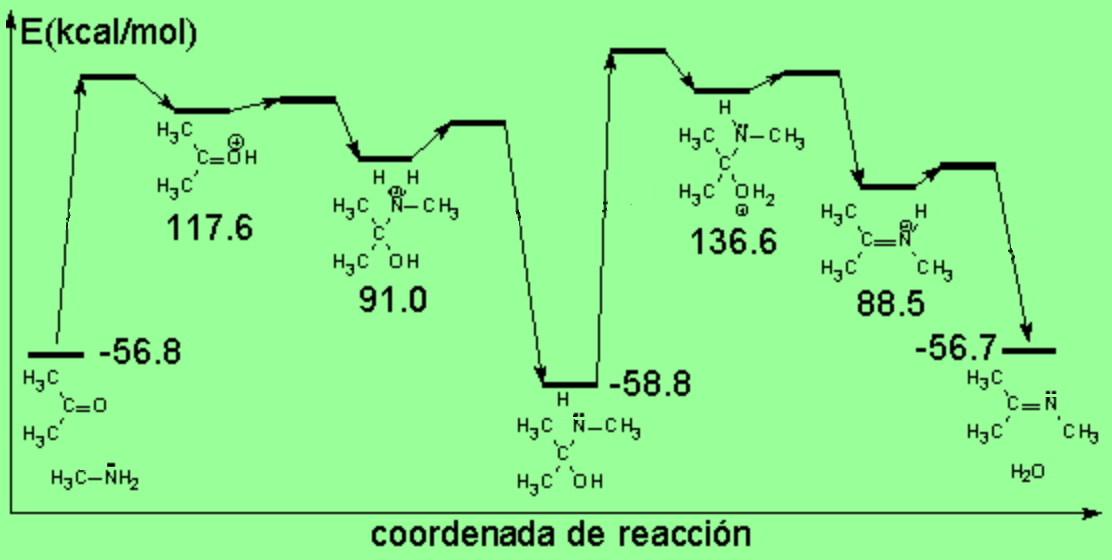
La catálisis ácida produce la protonación de algunas moléculas de cetona, aumentando la electrofilia del carbono carbonílico. Se produce entonces la adición nucleófila del nitrógeno amínico sobre el carbono carbonílico, que cambia de hibridación sp2 a sp3.
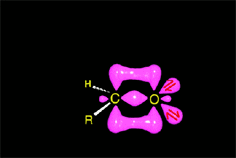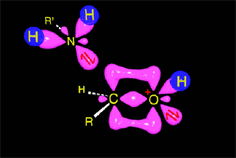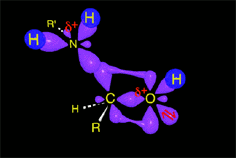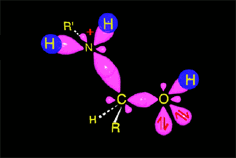
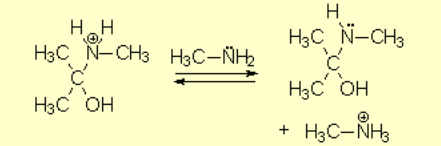 El intermedio tetraédrico protonado cede un protón a la amina que aun no ha reaccionado, produciendose un aminoalcohol geminal (ambas funciones sobre el mismo carbono) de alta estabilidad.
El intermedio tetraédrico protonado cede un protón a la amina que aun no ha reaccionado, produciendose un aminoalcohol geminal (ambas funciones sobre el mismo carbono) de alta estabilidad.
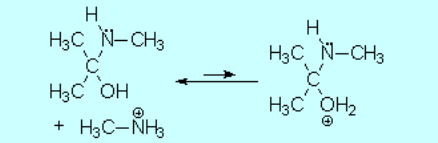 Parte de las moléculas de aminoalcohol sufren protonación en el OH, que es otro centro básico, dando lugar a un intermedio con un buen grupo saliente: el agua.
Parte de las moléculas de aminoalcohol sufren protonación en el OH, que es otro centro básico, dando lugar a un intermedio con un buen grupo saliente: el agua.
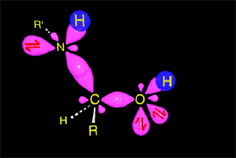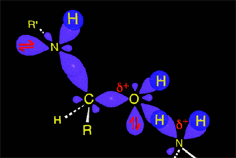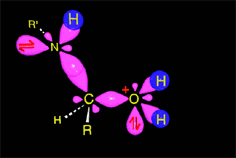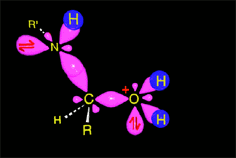
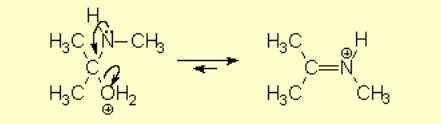 El enlace C-O debilitado por la protonación se rompe heterolíticamente, produciéndose la eliminación de agua y dando lugar a una sal de imonio intermedia. El carbono vuelve a recuperar la hibridación sp2.
El enlace C-O debilitado por la protonación se rompe heterolíticamente, produciéndose la eliminación de agua y dando lugar a una sal de imonio intermedia. El carbono vuelve a recuperar la hibridación sp2.
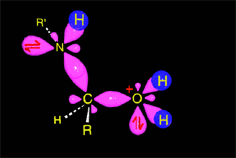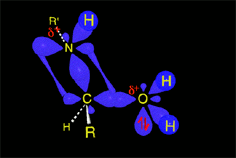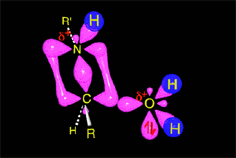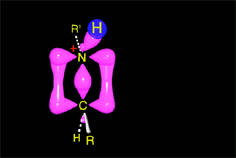
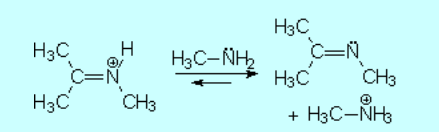 La amina en exceso desprotona la sal de imonio, obteniendose así la imina final.
La amina en exceso desprotona la sal de imonio, obteniendose así la imina final.