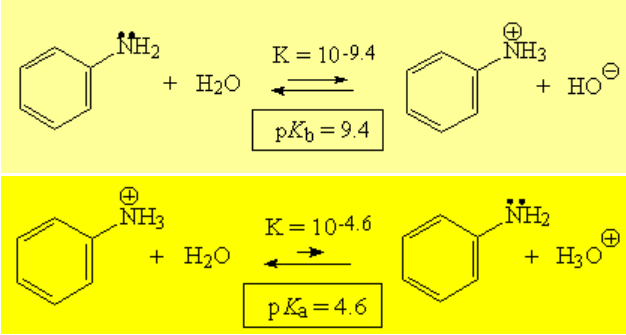
Las aminas aromáticas (anilinas) son menos básicas que las aminas y, por consiguiente, las sales de anilinio son más ácidas que las de amonio.
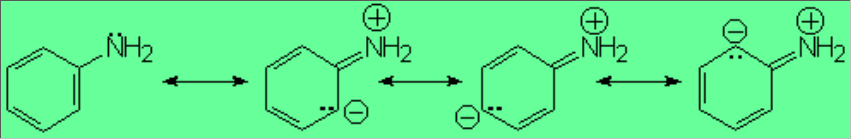
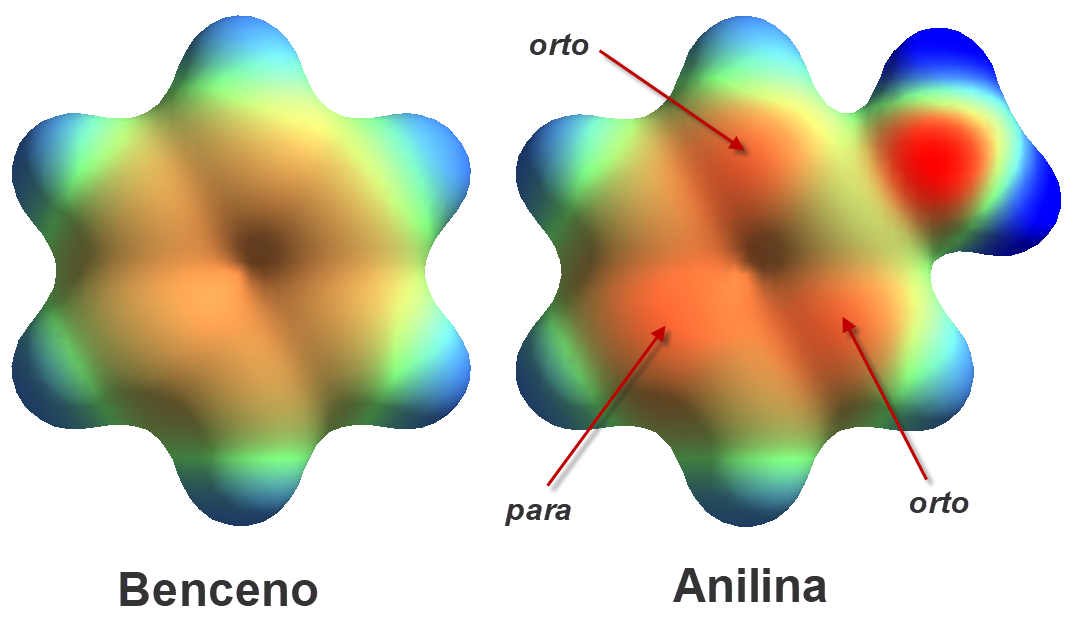
La razón la encontramos en las formas resonantes, que nos explican que el par de electrones de una anilina está menos disponible porque se deslocaliza hacia el anillo aromático. El cálculo de la densidad electrónica nos muestra como los carbonos en orto y para están "mas rojos" (mayor densidad electrónica) que en el benceno.