PROPIEDADES ÁCIDO-BASE DE COMPUESTOS CARBONÍLICOS:
ENOLIZACIÓN
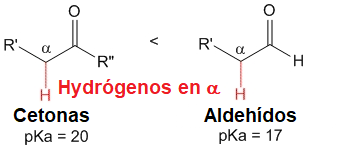
La posición alfa a un grupo C=O es mucho más ácida de lo esperado.
En relación a un alcano, el grupo C=O aumenta la acidez de su grupo CH contiguo en ¡¡¡ más de 30 órdenes de magnitud !!!
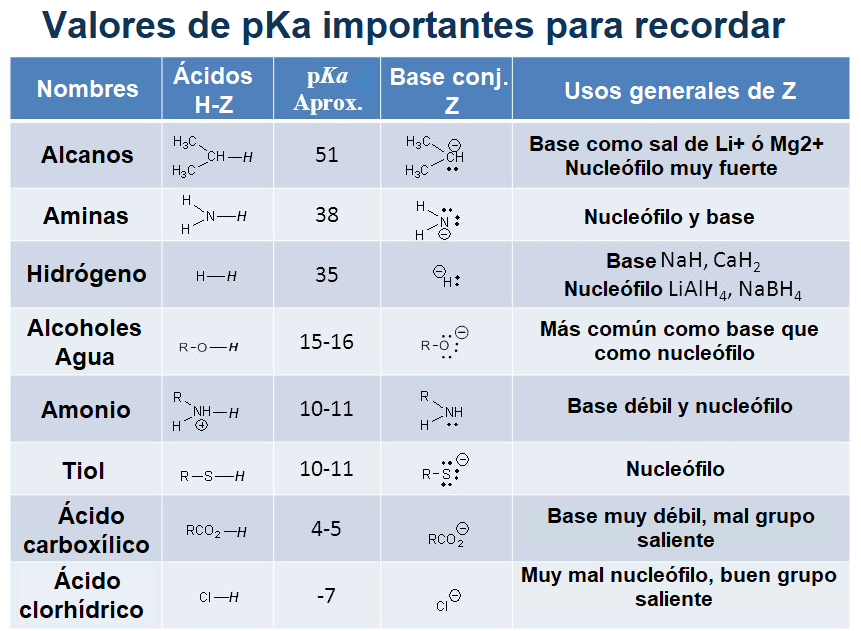
No viene mal recordar algunos valores de pKa.
Las bases que son capaces de desprotonar un alcohol también lo hacen sobre la posición alfa de un aldehído o cetona.
Pero date cuenta de que los aldehídos y las cetonas ya tienen la base dentro de sí mismas: ¡¡¡ el oxígeno del grupo C=O !!!.
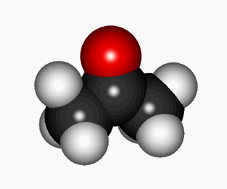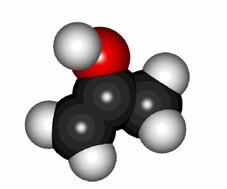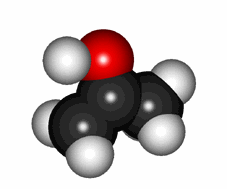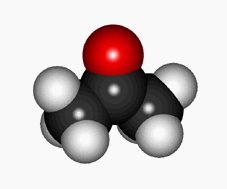
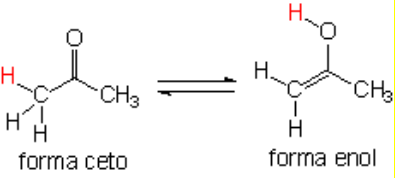
El oxígeno del grupo CH-C=O puede arrancarse a sí mismo el hidrógeno en alfa formándose así un enol.
Animación del equilibrio ceto-enólico
Equilibrio cetoenólico que está generalmente muy desplazado hacia la forma ceto en aldehídos y cetonas "normales".
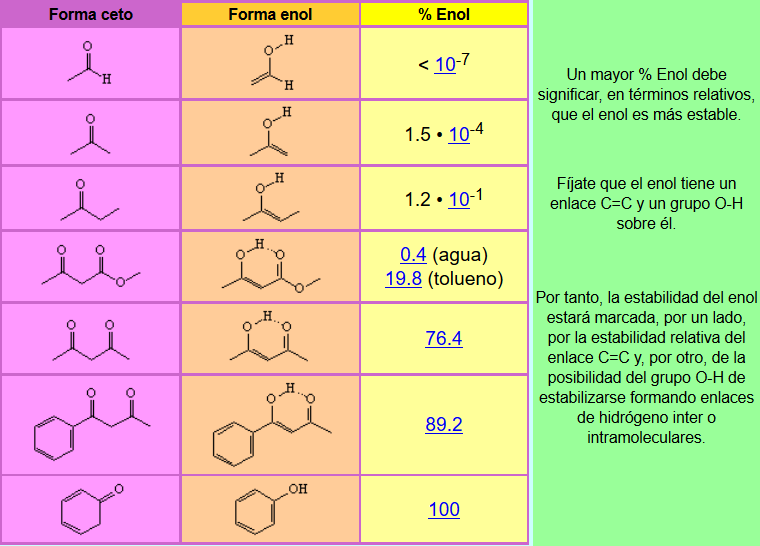
Es instructivo que analices la cantidad de enol en equilibrio que se ha medido experimentalmente para una serie de compuestos carbonílicos. ¿Puedes dar una explicación a las variaciones observadas en función de la estructura y el disolvente?
LA ENOLIZACIÓN DE ALDEHÍDOS Y CETONAS TIENE CONSECUENCIAS QUÍMICAS MUY IMPORTANTES
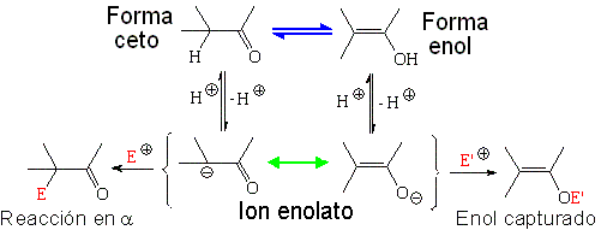
Fíjate que las formas ceto y enol son estructuras diferentes que están en equilibrio (flechas azules; hay un átomo que cambia de sitio), mientras que ion enolato sólo hay uno, que se describe mediante dos formas resonantes (flecha verde).
La reacción más común de un ion enolato se produce en posición alfa, dando lugar a un enalce C-C nuevo.
Algunas reacciones se producen por el oxígeno y permiten capturar el enolato. Recuerda esto para más adelante.