REACTIVIDAD DE ÁCIDOS CARBOXÍLICOS
El mapa de reactividad de un ácido carboxílico está marcado, en primer lugar, por la elevada acidez del OH y, en segundo, por la electrofilia del carbono carbonílico.
La relativa acidez de los hidrógenos en alfa, muy patente en otros derivados carbonílicos, queda totalmente enmascarada por la elevada acidez del grupo carboxilo.
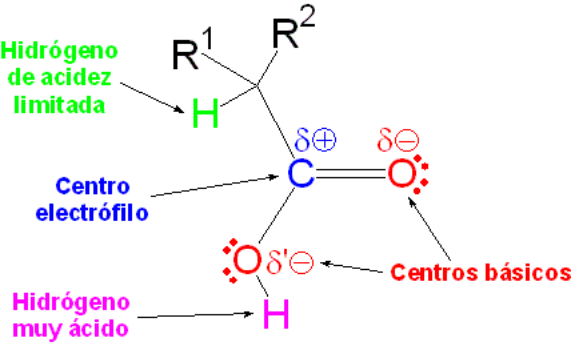
La acidez del grupo carboxilo suele interferir casi siempre en las reacciones que se quieran llevar a cabo en medio básico, neutralizando la base e impidiendo que se produzcan. Por tanto, el ataque nucleófilo al carbono carbonílico deberá hacerse, en general, en medio ácido.
El mecanismo de ataque a un ácido carboxílico o a un derivado suyo se denomina de adición-eliminación porque siempre consta de, al menos, esas dos etapas.
La etapa de adición ocurre primero y es seguida de otra de eliminación.
Mecanismo general de Adición-Eliminación
Las reacciones de los ácidos carboxílicos se llevan a cabo en medio ácido mineral o de Lewis. De esta forma se evita la interferencia de la acidez del grupo OH y se aumenta la electrofilia del carbono, al producirse la protonación parcial del grupo carbonilo, de propiedades básicas.
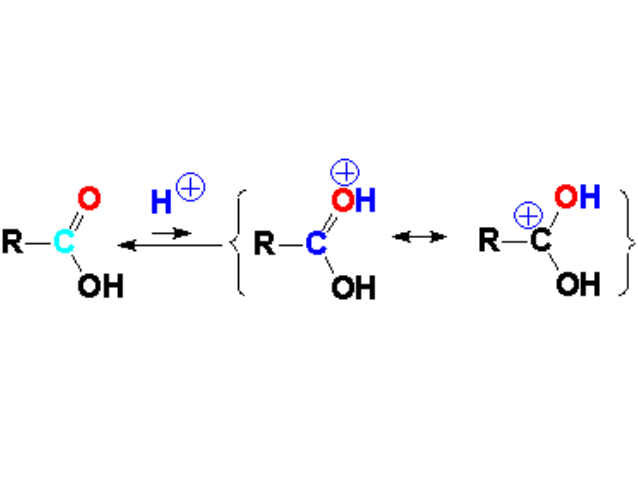
El oxígeno del grupo carbonilo tiene propiedades débilmente básicas. En presencia de un ácido mineral o de Lewis, las pocas moléculas que se protonen van a ser mucho más reactivas frente a un nucleófilo, ya que se aumenta la deficiencia electrónica del carbono carbonílico. Las formas resonantes así nos lo indican.
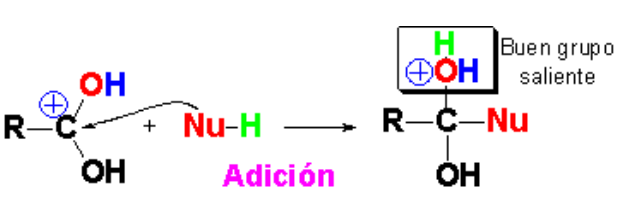
Se produce entonces la adición del nucleófilo, que debe ser protonado porque estamos en medio ácido.
En la etapa de adición el carbono inicialmente carbonílico cambia de hibridación sp2 (trigonal plana) a sp3 (tetraédrica).
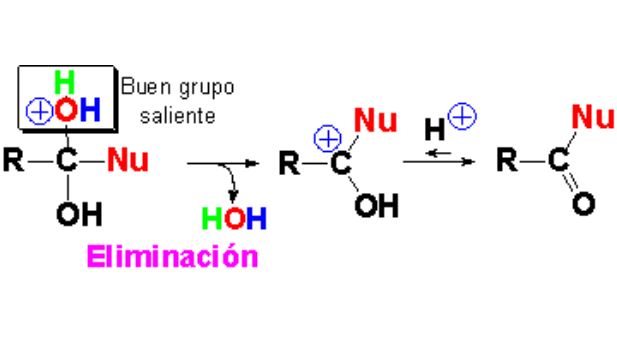
La molécula de agua incipiente formada en la etapa anterior se elimina con facilidad, dando lugar al derivado de ácido carboxílico, tras la pérdida de un protón.
En la eliminación el carbono reaccionante recupera de hibridación sp2. El protón utilizado inicialmente se recupera, por lo que la cantidad requerida de ácido para estas reacciones es catalítica.
Reacciones de Ácidos Carboxílicos