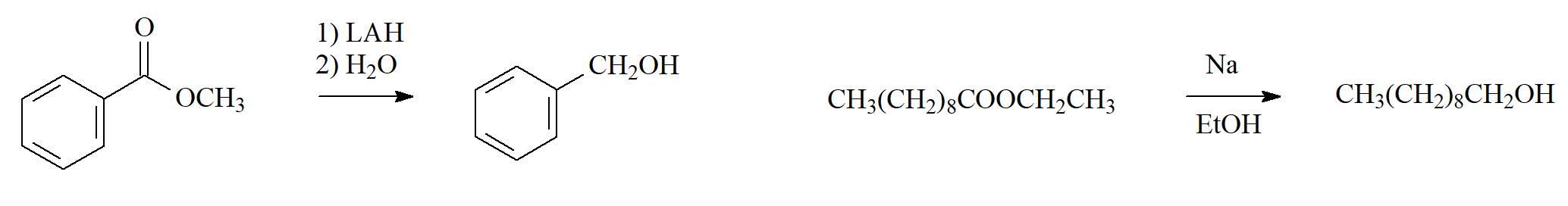Los ésteres son reactivos gracias a la electrofilia del carbono del grupo C=O y a su capacidad para estabilizar aniones enolato en posición alfa.
Esta reacción es la contraria a la esterificación de Fisher y su mecanismo es igual pero invirtiendo la secuencia (principio de reversibilidad microscópica).
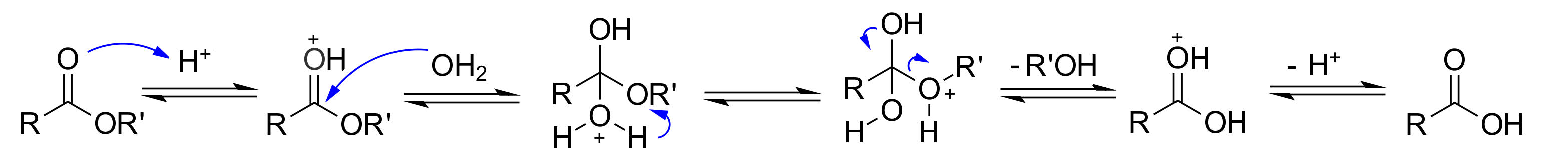
El mecanismo es el típico de adición-eliminación activado por la protonación inicial del grupo C=O.
Si se utiliza agua marcada isotópicamente con "18O" el alcohol no adquiere nada de marca isotópica lo que indica que el enlace indicado nunca se rompe y se corrobora el mecanismo de adición-eliminación.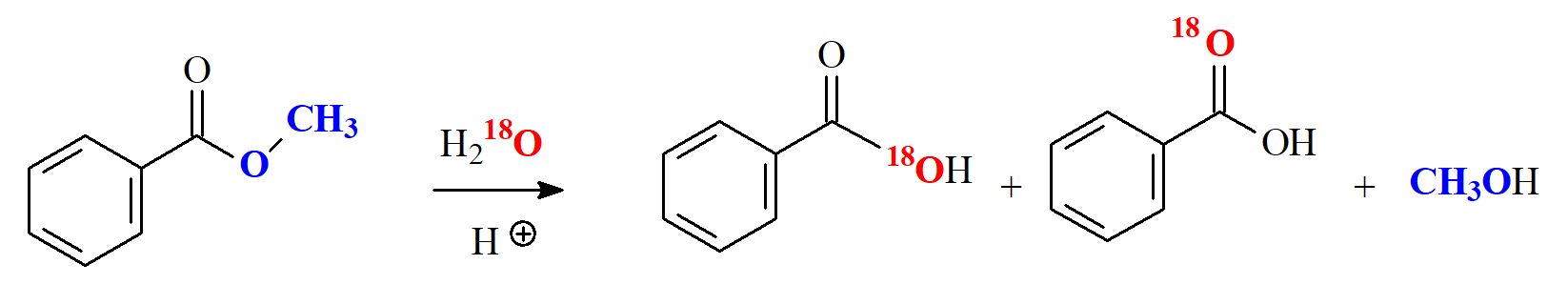
Hidrólisis Básica (Saponificación)
"Saponificación" significa "hacer jabón". La saponificación de las grasas es un método para obtener sales de carboxilatos de cadena larga.
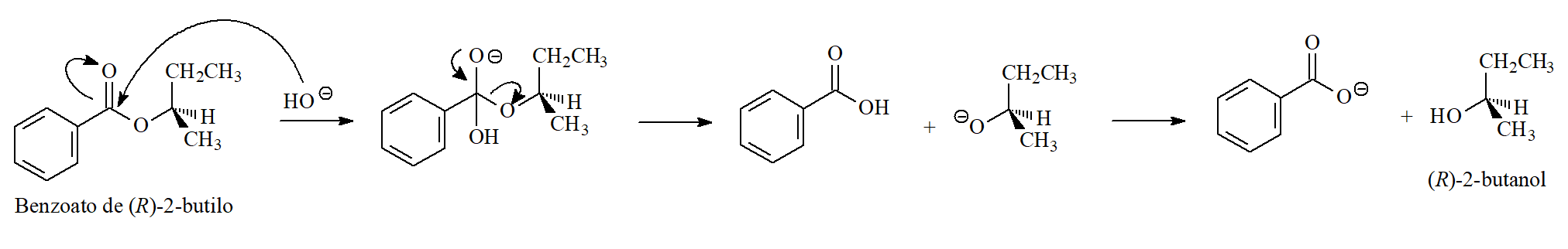
En el ejemplo siguiente la quiralidad de la parte alcohólica se mantiene intacta prueba nuevamente del mecanismo de adición-eliminación y de que el enlace entre el oxígeno y el resto alquilo nunca se rompe.
Si el hidróxido hubiera atacado al grupo butiloxi, o bien se habría invertido la configuración via un proceso SN2 o bien se habría racemizado via un mecanismo SN1.
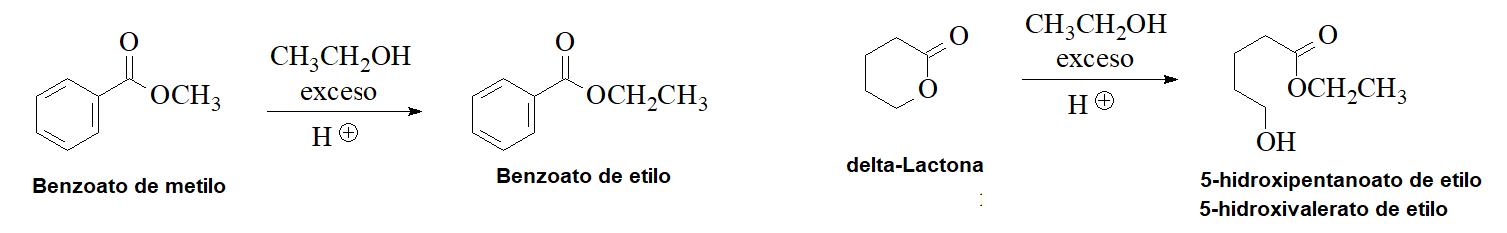
Transesterificación
Unos ésteres se pueden convertir en otros mediante su disolución en un alcohol en medio ácido. Mira algunos ejemplos:
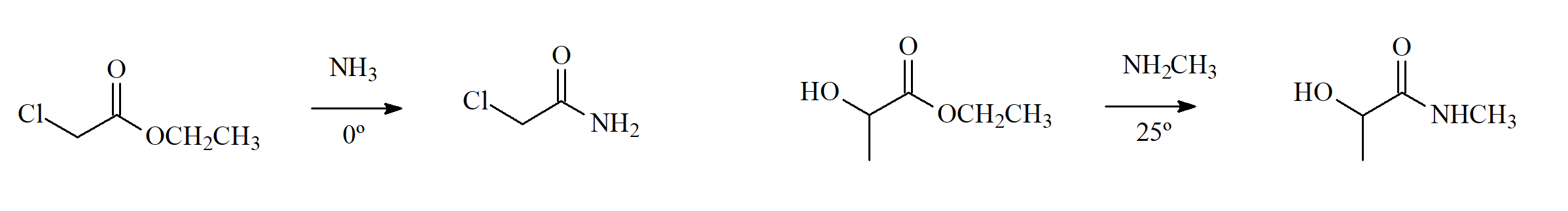
El amoníaco y las aminas primarias y secundarias (con N) son excelentes nucleófilos que reaccionan también con ésteres para dar amidas (con D).
¿Puedes proponer un mecanismo de adición-eliminación para este proceso?
Reducción con Hidruros o Metales
Los ésteres se reducen solo con hidruros enérgicos como el LiAlH4 (LAH).
El NaBH4 NO REACCIONA.
También pueden utilizarse metales alcalinos.
IMPORTANTE: ¡Precaución con la competencia de otros grupos!
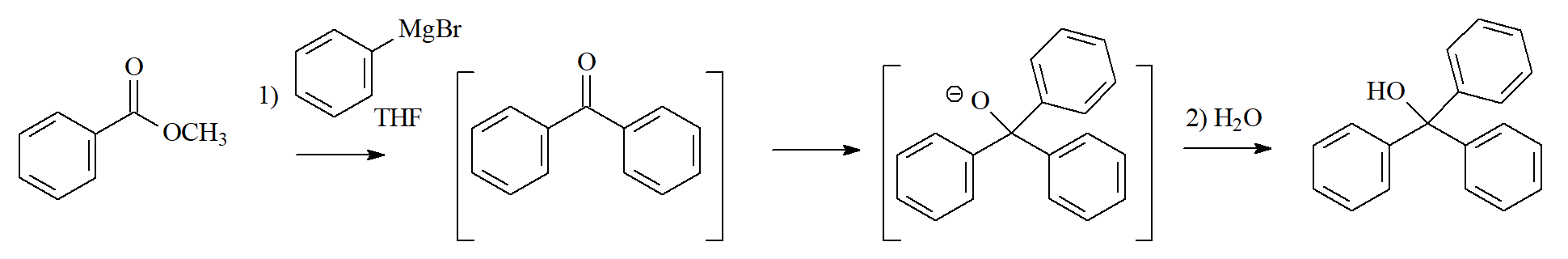
Reactivos de Grignard u Organolíticos
Los reactivos organometálicos reaccionan con ésteres mediante el mecanismo de adición-eliminación para formar alcoholes porque la cetona intermedia, más reactiva aun que el éster de partida, es atacada de nuevo por otra molécula de organometálico.
IMPORTANTE: ¡Precaución con la competencia de otros grupos funcionales!
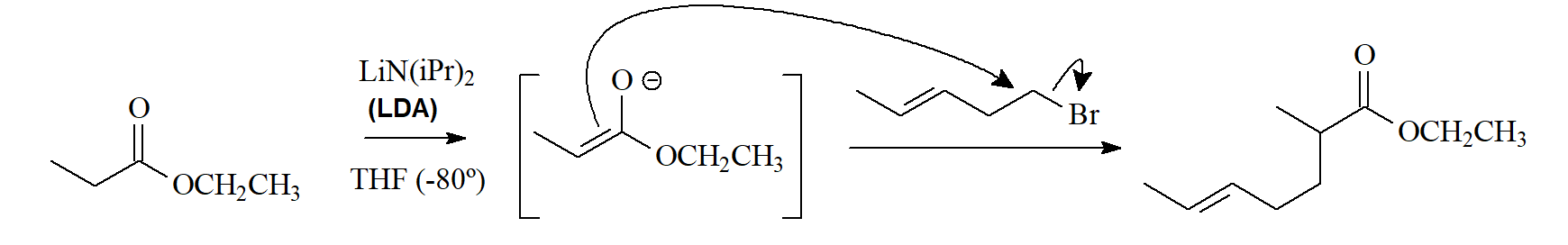
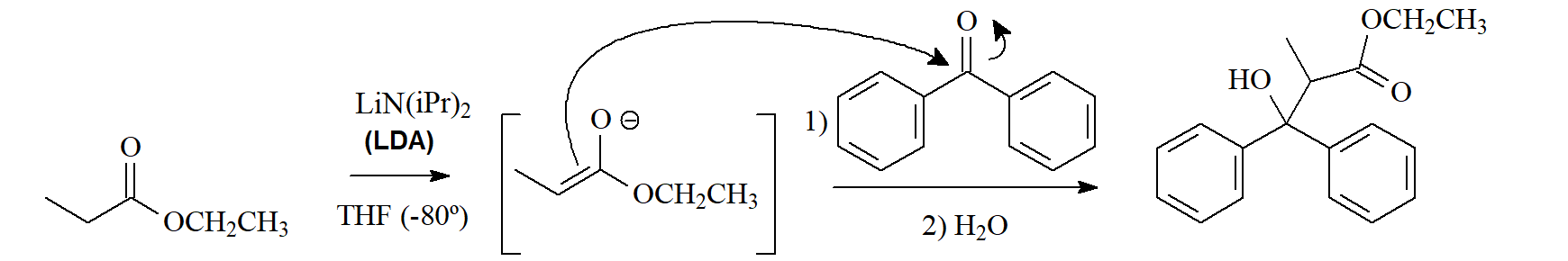
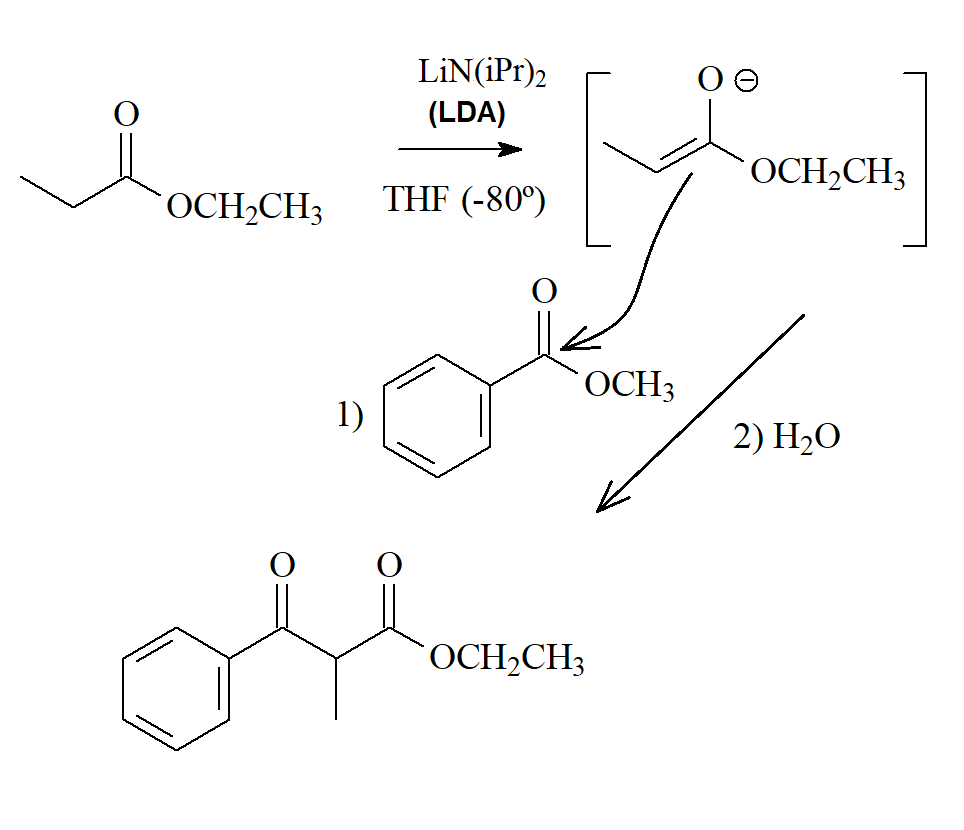
Los iones enolato de ésteres pueden dar varias reacciones:
1) SN (alquilación) con compuestos con un grupo buen saliente.
2) adición a otros grupos carbonilo
3) adición-eliminación a ésteres (condensación de Claisen)
La condensación de Claisen es a los ésteres lo que la condensación aldólica a aldehídos y cetonas.
Es muy importante porque permite la obtención de compuestos beta-dicarbonílicos que son muy versátiles en síntesis orgánica.
La condensación de Dieckmann es la versión INTRAmolecular de la condensación de Claisen.
Es muy importante porque permite la obtención de compuestos cíclicos beta-dicarbonílicos que son muy versátiles en síntesis orgánica.