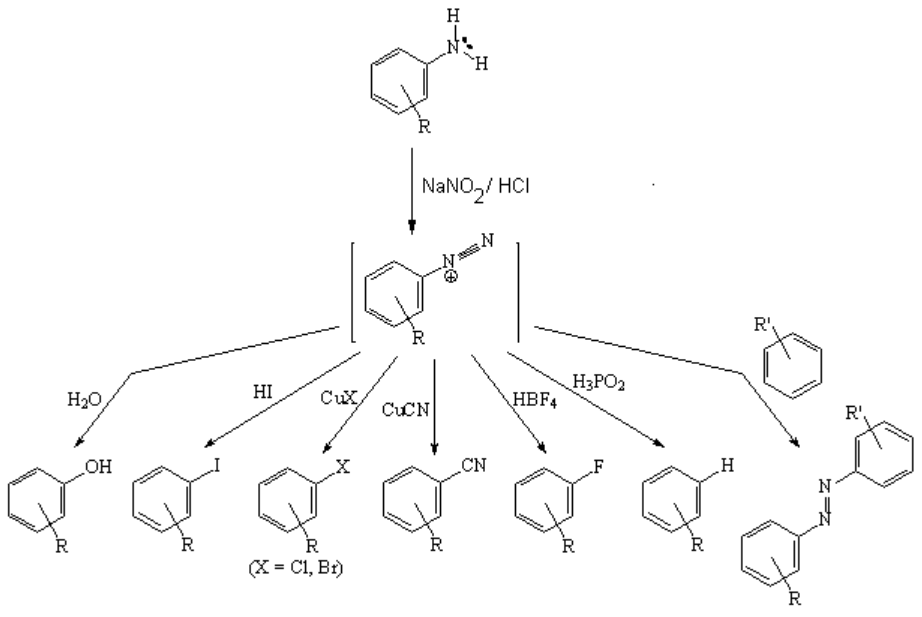
Las sales de diazonio son la puerta de entrada a hidrocarburos aromáticos con una enorme cantidad de funciones orgánicas diferentes.
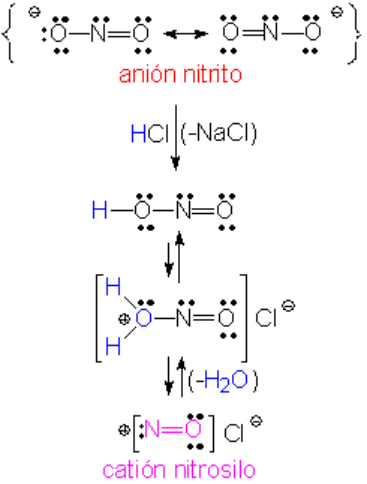
El anión nitrito es suficientemente básico para reaccionar dos veces con un ácido mineral como el clorhídrico. La doble protonación permite la pérdida de una molécula de agua, obteniendose así el catión nitrosilo, fuertemente electrófilo y muy reactivo. Este catión se crea "in situ", es decir, en presencia de la anilina.
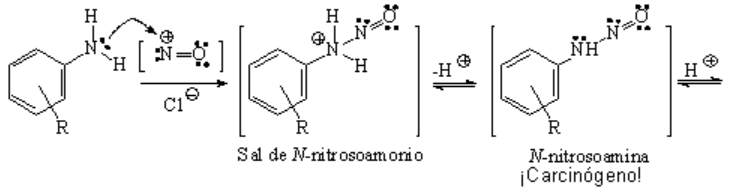
El nitrógeno de las anilinas, muy nucleófilo, puede reaccionar fácilmente con el catión nitrosilo. Esta reacción da lugar a una cascada de intermedios que finalmente conducen a una sal de diazonio
En un primer paso, el par de electrones de la amina se une al centro más deficiente en electrones del catión nitrosilo, que es el nitrógeno. Se pierde un protón y se obtiene una N-nitrosoamina, producto peligroso por sus propiedades carcinogénicas
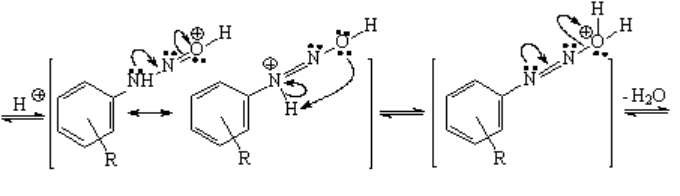
La N-nitrosoamina tiene numerosos pares de electrones sin compartir, por lo que es básica. No olvidemos que el catión nitrosilo ha sido creado "in situ" mediante el medio ácido. Este medio es capaz de protonar la N-nitrosoamina que, al final, pierde una molécula de agua.
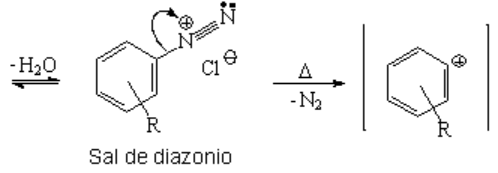
La pérdida de agua da lugar a la sal de diazonio, que hay que almacenar con cuidado ya que tiende a perder nitrógeno, de forma explosiva, con facilidad. Si esta reacción se controla, en presencia de un nucleófilo, el grupo N2 puede reemplazarse casi por cualquier otra cosa (mira arriba).