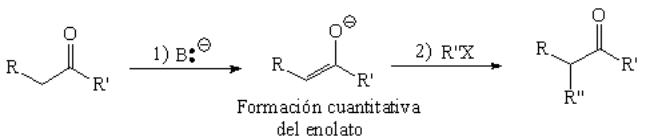
Los enolatos cargados negativamente y por tanto con exceso de electrones, son buenos nucleófilos para producir reacciones de sustitución nucleófila sobre un compuesto apropiado que contenga un buen grupo saliente.
La consecuencia de esta reacción es la alquilación del aldehído o cetona en posición alfa, aumentandose así la complejidad de la molécula original.
La base ha de ser fuerte para transformar el aldehído o cetona 100% en su enolato.
Habitualmente se utilizan:
Hidruros metálicos (NaH)
Alcóxidos (t-BuOK)
Amiduros [NaNH2 o LiN(i-Pr)]
Los disolventes han de ser inertes, como el dimetoxietano -DME-, la dimetilformamida -DMF-, el tetrahidrofurano -THF- y la hexametilfosforotriamida -HMPT-.
Esta reacción tiene algunos problemas:
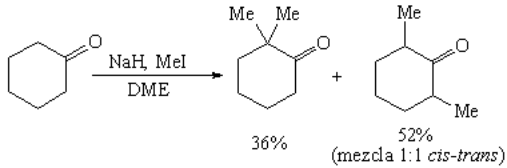 La polialquilación de cetonas simétricas es difícil de evitar, incluso utilizando un mol de agente alquilante.
La polialquilación de cetonas simétricas es difícil de evitar, incluso utilizando un mol de agente alquilante.
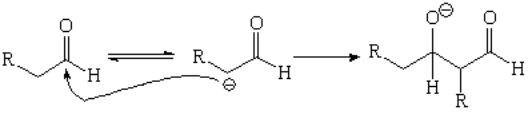 Los aldehídos, en vez de alquilarse, suelen reaccionar consigo mismos dando una reacción que veremos a continuación: la condensación aldólica.
Los aldehídos, en vez de alquilarse, suelen reaccionar consigo mismos dando una reacción que veremos a continuación: la condensación aldólica.
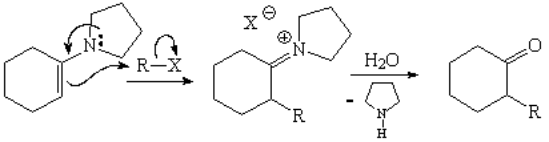
La mejor manera de evitar estos problemas y conseguir monoalquilaciones regioselectivas es la utilización de enaminas.
Ahora podemos observar las enaminas con una perspectiva práctica: como si fueran enolatos estables sin carga formal, cuya formación no implica la presencia de una base fuerte.
Las enaminas son menos reactivas que los iones enolato y por ello permiten realizar una monoalquilación regioselectiva sin los problemas anteriores.
¡Utiliza enaminas SIEMPRE que quieras efectuar la alquilación de un aldehído o cetona!
 La polialquilación de cetonas simétricas es difícil de evitar, incluso utilizando un mol de agente alquilante.
La polialquilación de cetonas simétricas es difícil de evitar, incluso utilizando un mol de agente alquilante.
 Los aldehídos, en vez de alquilarse, suelen reaccionar consigo mismos dando una reacción que veremos a continuación: la condensación aldólica.
Los aldehídos, en vez de alquilarse, suelen reaccionar consigo mismos dando una reacción que veremos a continuación: la condensación aldólica.